이전 글은
원소, 원자, 분자의 구분에 대한 내용이었습니다
2023.01.15 - [과학/중학교 과학2] - 중2 과학 - 물질의 구성 - 원소, 원자, 분자의 구분
중2 과학 - 물질의 구성 - 원소, 원자, 분자의 구분
이번 글은 중학교 2학년 1학기에 주로 배우는 물질의 구성 단원 원소, 원자, 분자에 관한 내용입니다. 원소, 원자, 분자를 명확하게 구분하여 사용하는 사람은 많지 않습니다 (혼용해서 사용합니
musics.tistory.com

이번글은
원자의 구조와
원자 모형의 발달에 대해 설명하고
원자를 구성하는 요소들에 대한
다양한 성질에 대해 이야기하려합니다
글의 순서는
1. 원자의 구조
2. 원자모형의 변화
입니다
1. 원자의 구조
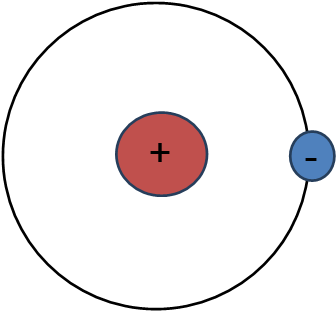
보통 중학교에서는
중심에 원자핵이 있고
그 주위에 전자가 돌고 있는 것으로
묘사합니다.
원자핵은
원자의 거의 모든 질량을 차지하고 있습니다
하지만 그 크기는 아주 작죠
예를 들면 축구장이 있다면
축구장 중심에
축구공하나보다 작은 크기(10만 분의 1가량)
정도라고 생각하면 됩니다.
보통 책에는 위 그림처럼 나오는데
실제로 비율로 그리면
책에 넣을 수 없어서 위에 그림처럼 그립니다
전자는
원자핵주변을 돌고 있다고
많이 표현합니다
물론 현대과학에서는 그렇게 말하지 않지만
중학교에서는
'전자는 원자핵주변을 빙빙 돌고 있다'
로 알고 있어도 문제는 없습니다.
원자핵과 전자를 비교 해보면
다음과 같습니다
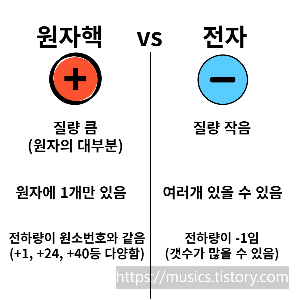
일단 전기적성질을 둘 다 가집니다
원자핵은
전기적으로 +전하를 띄고 있습니다
전자는
전기적으로 -전하를 띄고 있습니다.
원자핵의 전하량(+의 정도)은
+1, +2, +3 등 종류에 따라 다양합니다
원자핵의 전하량에 따라
원소 종류가 다르다고 생각하면 됩니다
전자는 전하량이 항상 -1 이고
보통 원자핵의 +만큼
원자 내부에 존재하여
원자 외부에서 볼 때
전하량이 0 (중성)으로 보이게 합니다
즉, 원자핵이 +6인 원자는
전자 6개를 가지고 있어서
외부에서 볼 때 전하량이 0이 됩니다
전하량이 0인 경우를
전기적으로 중성이라고 합니다
정리
원자의 구조는
원자핵과 전자로 구성되어 있다
원자핵이
원자 대부분의 질량을 차지하고 중심에 있으며
원자핵의 전하량만큼의 전자가
주변에 존재한다
2. 원자모형의 변화
원자 구조 모형의 변화
눈에 보이지 않고
현미경으로도 볼 수 없는 원자의 구조
어떻게 사람들이 알게 되었을까요?
보통 중학교에서는 다루지 않지만
이해를 돕기 위해
간단하게 변화 과정을 설명하겠습니다
1) 돌턴의 모형 (공모형)

위의 모형은 초창기 원자의 모형입니다
단순한 공 모형입니다
돌턴이라는 사람이 주장하였습니다.
뭐가 대단하냐고 하실 수 있으나
눈에 보이지도 않는
아주 작은 알갱이의 존재를
예측해 낸 것 자체가
대단하다고 생각합니다
물론 데모크리토스라는 고대 학자가
원자라는 명칭을 먼저 제시하기는 하였습니다만
원자 모형의 초기는
돌턴의 원자모형으로 많이 제시됩니다
2) 톰슨의 모형(건포도 빵 모형)
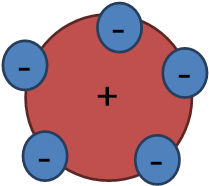
JJ톰슨이라는 아저씨가 제안한
건포도 빵 모형입니다
빵 중 건포도가 박힌 빵처럼
- 전하인 전자들이 +전하인 원자에
박혀있는 모형이 제시됩니다
톰슨은
'원자가 +와 -를 가진 물질로 구성되어 있다'
는 걸 제시한거죠
단순히 감으로 맞춘게 아니라
실제로 전자의 존재를 밝혀내고
그 공로로 노벨상을 받기도 합니다.

3) 러더퍼드의 모형과 보어의 모형
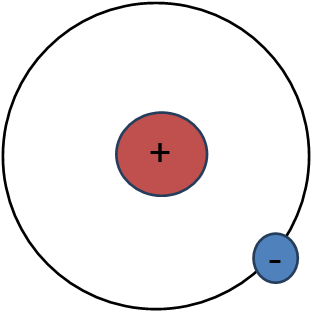
러더퍼드의 모형과
보어의 모형은 약간은 다르지만
전자가
원자핵의 주변을 돈다는 부분에서
비슷하여 하나로 묶었습니다
러더퍼드라는 사람은
원자에 뭘 자꾸 쏘는 실험을 합니다
알파입자산란실험이라고 불리는 그 실험에서
러더퍼드는
+전하를 띈 아주 질량이 큰 (원자기준) 핵이
중심부에 있고
원자의 대부분 공간은
텅텅비어 있다는 사실을 밝혀냅니다
이에 위와 같은 모형을 제시하게됩니다
보어는
나중에 원자핵 주변의 전자들이
그냥 도는게 아니라
돌 수 있는 궤도가 정해져 있다는 것을 제안합니다
실험 결과에서
원자가 특정 에너지의 빛을 흡수하고 방출하는데
이를 설명하기 위해 도입하고
이를 통해 전자의 에너지가
양자화 되어 있음을 주장합니다
너무 어려운 내용이라
중학교 수준에선 그런가보다로 가셔도 됩니다
보어의 모형을 이용하면
원자의 스펙트럼(빛의 띠)를 설명할 수 있습니다.
4) 현대 모형
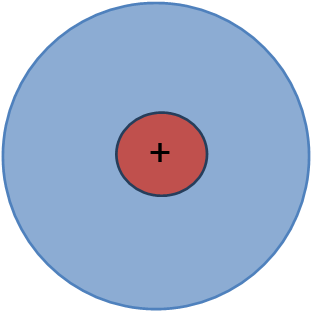
위쪽 그림의 빨간색 +는
원자핵을 나타냅니다
그리고 주변의 반투명한 파란 부분은
전자가 파동의 형태(확률)로 존재함을 나타냅니다
현대 과학의 양자역학은
모든 것은 확률적으로 존재한다고 봅니다.
이에 원자에 존재하는 전자들도
입자로 존재하는 것이 아니고
확률적으로 존재하여
관측되었을 때 나타난다고 봅니다
그래서 현대 모형에서는
원자핵과 전자확률구름으로 구성되어 있다고
제시합니다
정리
우리가 당연하게 배우는 원자의 구조는
실제로 수 많은 과학자들의 연구의 산물입니다
단순히 외우기 보다 과정을 안다면
구조를 외우기가 좀 더 쉽습니다
이번글에서는
원자의 구조와 원자모형의 발달과정에 대하여
이야기 하였습니다
눈에 보이지 않는 세계이기 때문에
신기하기도 하지만
재미가 없을 수도 있다고 생각합니다
하지만 수많은 눈에 보이는 결과는
이런 보이지 않는 것에서
시작되는게 아닐까요?
감사합니다.
다음으로 보면 좋은 글은
2023.01.29 - [과학/중학교 과학2] - 중2 과학-물질의 구성-불꽃반응 실험, 불꽃색, 원자와 빛의 스펙트럼의 관계
중2 과학-물질의 구성-불꽃반응 실험, 불꽃색, 원자와 빛의 스펙트럼의 관계
도입 이번글에서 다룰 내용은 -불꽃반응 실험, 불꽃색 -불꽃색이 나타나는 이유 -스펙트럼 등을 원자의구조(보어모형)으로 설명하려합니다. 1. 불꽃 반응실험, 불꽃색 불꽃 반응 실험: 특정한 원
musics.tistory.com
또는
2023.01.28 - [과학/중학교 과학2] - 중2 과학 - 물질의 구성 - 분자
중2 과학 - 물질의 구성 - 분자
도입 분자라는 단어는 일상생활에서도 많이 들어볼 수 있는 익숙한 단어 입니다. 친구와 말싸움을 할 때 '너를 분자단위로 쪼개버리겠다' 라든가 요리프로그램에서 보이는 '분자요리'라던가 분
musics.tistory.com
입니다.
도움이 되셨기를 바랍니다
감사합니다
'과학 > 중학교 과학2' 카테고리의 다른 글
| 중2 과학-물질의 구성- 이온, 이온의 형성, 이온의 종류와 특성, 양이온, 음이온) (0) | 2023.01.30 |
|---|---|
| 중2 과학-물질의 구성-원소기호, 분자식 읽는 법. (1) | 2023.01.29 |
| 중2 과학-물질의 구성-불꽃반응 실험, 불꽃색, 원자와 빛의 스펙트럼의 관계 (0) | 2023.01.29 |
| 중2 과학 - 물질의 구성 - 분자-정의와 예시, 분자모형예시 (0) | 2023.01.28 |
| 중2 과학 - 물질의 구성 - 원소, 원자, 분자의 구분 (0) | 2023.01.15 |




댓글