이전 글은 원자에 관한 내용입니다
2023.01.15 - [과학/중학교 과학2] - 중2 과학 - 물질의 구성 - 원소, 원자, 분자의 구분
중2 과학 - 물질의 구성 - 원소, 원자, 분자의 구분
혹시 글이 도움이 되신다면 잠시 시간을 내어 하트와 광고 클릭을 부탁드립니다 필자에게는 큰 힘이 됩니다 감사합니다 이번 글은 중학교 2학년 1학기에 주로 배우는 물질의 구성 단원 원소, 원
musics.tistory.com
이번글은
원소기호, 분자식에 관한 내용입니다.



물이나 산소, 이산화탄소 같은 경우
분자식을 접하기가 쉽습니다
하지만 지구에는 우리가 모르는 분자가 더 많습니다.
언어가 다르면 소통이 안되듯
과학자들은 소통을 위해
공통으로 쓰는 원소기호를 사용합니다.
1. 원소기호
원소기호는 과학자들 사이에서의 약속입니다.
아래표와 같이 공통적으로 사용합니다.
여기서 중요한건 원자번호와 원소이름, 그리고 원소기호입니다.
중학교 2학년에서는 보통 20번 정도까지는 외웁니다.
하지만 막상 많이 들어본 이름이 많아서 외우는데 어려움은 없습니다.
| 원자번호 | 기호 | 원소이름 | 영어 이름 | 라틴어 이름 | 영어 이름 유래 |
| 1 | H | 수소 | Hydrogen | Hydrogenium | 고대 그리스어:hydro- + gen물 생성 |
| 2 | He | 헬륨 | Helium | Helium | 고대 그리스어:helios태양 |
| 3 | Li | 리튬 | Lithium | Lithium | 고대 그리스어:lithos돌 |
| 4 | Be | 베릴륨 | Beryllium | Beryllium | 광물:녹주석(beryl) |
| 5 | B | 붕소 | Boron | Borium | 광물:붕사(borax) |
| 6 | C | 탄소 | Carbon | Carbonium | 라틴어:carbo석탄 |
| 7 | N | 질소 | Nitrogen | Nitrogenium | 광물:질산염(nitrum)(고대 그리스어:nitron + -gen (질산염 생성)) |
| 8 | O | 산소 | Oxygen | Oxygenium | 고대 그리스어:oxy + -gen산 형성 |
| 9 | F | 플루오린 | Fluorine | Fluorum | 광물:형석(라틴어:fluere) |
| 10 | Ne | 네온 | Neon | Neon | 고대 그리스어:neos새로운 |
| 11 | Na | 나트륨 | Sodium | Natrium | 영어:soda,라틴어:natrium |
| 12 | Mg | 마그네슘 | Magnesium | Magnesium | 광물:산화 마그네슘(지역:그리스동테살리아마그네시아지방) |
| 13 | Al | 알루미늄 | Aluminium | Aluminium | 광물:명반석(alum),산화 알루미늄(alumina) (원어: aluminum) |
| 14 | Si | 규소 | Silicon | Silicium | 고대 그리스어:silexsilex, silicis부싯돌(원어: silicium) |
| 15 | P | 인 | Phosphorus | Phosphorus | 고대 그리스어:phos + phoros빛 운반체 |
| 16 | S | 황 | Sulfur | Sulphur | 라틴어:sulphur불과 유황, 업화(業火) |
| 17 | Cl | 염소 | Chlorine | Chlorum | 고대 그리스어:chloros녹황색 |
| 18 | Ar | 아르곤 | Argon | Argon | 고대 그리스어:argos비활성 |
| 19 | K | 칼륨 | Potassium | Kalium | 신라틴어: potassa칼리(라틴어:kalium) |
| 20 | Ca | 칼슘 | Calcium | Calcium | 라틴어:calx석회 |
원소와 분자의 연구가 활발했던 시대에는
연금술사라는 사람들이
연금술( 금을 만들어내는 기술)을 연구하였고
이 연구들이 근대 화학의 발전에 큰 도움이 되었습니다.
그 당시에는 연구의 발견물인 원소와 분자는
자신의 업적으로 다른 사람들에게 비밀로하기 위해
각기 다른 문자를 이용해 기록했었지만
나중에 기호를 통일하게 됩니다
2. 분자식 해석하기
분자는 단원자분자라는 특이 케이스를 제외하고
두개 이상의 원자의 결합으로 이루어져있습니다.
(단원자 분자는 원자 하나로 분자의 성격을 가집니다)
어떤 물질인지 모르더라도
분자식을 분석하여
어떤 원소 구성인지 알 수 있습니다.
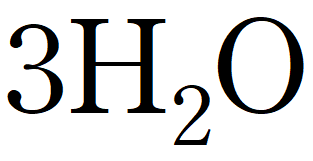
위의 분자식을 보겠습니다
숫자가 두개가 있습니다
문자의 오른쪽아래에 작은 숫자는
왼쪽에 있는 원소의 갯수를 의미합니다
1은 생략합니다.
분자의 제일 앞의 숫자는
분자의 갯수를 의미합니다
1은 생략합니다
분자식을 보면
2개의 수소(H)원자와 1개의 산소(O)원자가 합해진 분자이고
그 분자가 3개 있다는 것을 알 수 있습니다
여기서 여러가지 질문으로 이어질 수 있습니다.
1) 위 식에서 물분자는 몇개 인가요?
-> 3개입니다. 분자의 제일 앞의 숫자가 분자의 갯수를 의미합니다.
2) 위 식에서 총 몇종류의 원소가 존재하나요?
->2종류입니다.
3) 위 식에서 총 몇개의 수소원자가 있나요?
-> 6개 입니다
분자 한개 당 2개의 수소원자가 있는데
그런 분자가 3개가 있어 3x2=6으로 유추할 수 있습니다.
원소기호의 종류와 분자식에 대하여
간단하게 정리하였습니다.
실제 우리가 만나는 분자는
훨씬 복잡한 형태이므로
중학교에서는 간단한 형태만 보게 됩니다.
다음글에서는
이온의 형성과 이온의 특성에 대하여
이야기하려 합니다
2023.01.30 - [과학/중학교 과학2] - 중2 과학-물질의 구성- 이온 (이온의 형성, 이온의 종류와 특성, 양이온, 음이온)
중2 과학-물질의 구성- 이온 (이온의 형성, 이온의 종류와 특성, 양이온, 음이온)
중학교 2학년이 처음 배우는 내용은 원자, 분자, 원소 입니다. 이온은 원자의 구조를 이해하고 한가지 요소를 더 이해하고 배우면 좋습니다. 이번 글에서는 이온의 형성과 이온의 표현법에 대하
musics.tistory.com
도움이 되셨기를 바랍니다
감사합니다.
'과학 > 중학교 과학2' 카테고리의 다른 글
| 중2 과학-물질의 구성-앙금생성반응 실험, 이온결합, 숨은 이온 찾기 (0) | 2023.01.31 |
|---|---|
| 중2 과학-물질의 구성- 이온, 이온의 형성, 이온의 종류와 특성, 양이온, 음이온) (0) | 2023.01.30 |
| 중2 과학-물질의 구성-불꽃반응 실험, 불꽃색, 원자와 빛의 스펙트럼의 관계 (0) | 2023.01.29 |
| 중2 과학 - 물질의 구성 - 분자-정의와 예시, 분자모형예시 (0) | 2023.01.28 |
| 중2 과학 - 물질의 구성-원자의 구조. 원자핵, 전자, 원자모형의 변화 (0) | 2023.01.15 |




댓글